|
トロトラスト処置を受けた患者のガン組織、 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ◆ 論文で紹介します(翻訳:伊澤) ◆ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
P53 mutations in tumor and non-tumor tissues of Thorotrast recipients : a model for cellular selection during radiation carcinogenesis in the liver. Takesaburo Mori 放射線医学研究所 日本 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
トロトラストは、二酸化トリウムを含むコロイドで造影剤として20世紀始めから世界中で使われて、日本では、1960年代後半まで使われて、非常に高い確率で血液や肝臓のガンを発生させました。トリウムは半減期100億年で、トリウムが崩壊して生じる娘核種のほとんどはα線を放出し、処置された患者の生涯にわたり沈着した狭いエリアにα線を照射し続ける。 血管内注入されたトロトラストの90%以上は体内に、そしてその60%以上は肝臓に滞った。器官線量は、1年当たり0.1〜0.7グレイと計算された。患者の多くは若い兵士だったので、生涯線量は35グレイ以上の可能性がある。この様な、低線量率ではあるが総計では高線量に達するα線被曝が正常細胞をガン化させるメカニズムについては分かっていない。 急性被曝と違い、慢性被曝はある細胞がガン化する過程を通して、ずっとダメージを与え続ける。さらにα線は、X線やγ線とは異なっているので、一部の研究者達はα線に固有な影響を論じている。α線被曝による発ガンの初期及び後期を分析するために、P53ガン抑制遺伝子をトロトラストによって生じたガン組織と非ガン組織で分析した。P53はヒトガン細胞で突然変異していることが多い遺伝子の1つです。ヒトのガンではP53遺伝子の突然変異は発ガンの後期段階で生じると考えられていますが、肝発ガンでは、初期段階に見られるという報告もあります。さらに、P53遺伝子の正常機能の喪失は、増殖コントロールを失わせることが知られているので、私達の仮説は、特定のDNAの傷害を受けた細胞が生き残り、その変異を保持したまま増殖している組織がガンにも非ガン組織にも存在している、というものです。他の言い方をすれば、ガン化した組織にのみ突然変異が生じているわけではなく、ガン化していない組織にも遺伝子の変異が生じている、両組織とも被曝による遺伝子の突然変異を示しているということです。我々の研究結果はこの仮説を支持しており、ヒト、ガンでみつかったことは放射線によってゲノム(遺伝子全体)が不安定化しているということだ。 我々が見つけた数多くのP53遺伝子の突然変異は、α線がP53遺伝子を直接照射した結果ではなく、α線照射は、細胞内環境をゲノム不安定化を促進する方向に変え、それによってP53遺伝子を欠失させたりしている、というモデルを提唱する。 私達は、トロトラスト処置を受け、ガンを発症した20人の患者のP53ガン抑制遺伝子を分析した。20人の内、19人がP53遺伝子の点突然変異を持っていた。さらに、これらの患者の非ガン組織からも、頻度は低いもののP53の突然変異がみつかった。私達の結果はトロトラストによる発ガンにおいて、P53突然変異が重要であるが、これらの突然変異は、α線照射によって(直接起こったものではなく)2次的なゲノムの不安定化によるものだという説を支持している。
解 説
表2.トロトラスト投与患者の調査結果
表3.わが国のトロトラスト血管内注入剖検例での肝線量率、肝悪性腫瘍発生数および注入より死亡までの期間の関係
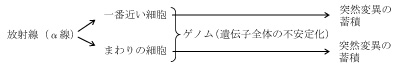
表2.日本255人中肝腫瘍死56人、白血病死6人とものすごい高い割合でガン死が起きています。表3をみると、それが30.7年から42.5年もの長い潜伏期間を経て、ガンが生じて死亡していることがわかります。トロトラスト中のトリウムは、α線を出し続け、トリウム粒子の近辺の細胞に傷害を与え続けます。この論文が示していることは、私達が知っているガン化の経路、遺伝子の突然変異(イニシエーション)→プロモーション→プログレッションという経路でガン細胞が突然変異を重ねていって悪性化していくという考え方の他に、
という、α線によるゲノムの不安定化によるガンの発達という新しい経路がありうるということを立証したものです。 P53遺伝子は、ガン抑制遺伝子の1つであり、細胞分裂をコントロールしている遺伝子で、DNAに切断などの突然変異を受けた細胞などでは、DNAを修復するまでは、細胞分裂を止める働きをしています。その遺伝子が偶然に突然変異して、ガン化していく経路とは異なり、放射線によりゲノム(遺伝子全体)が不安定化し、DNA修復などが起きにくくなり、突然変異を蓄積していく経路がありうる、といっています。 放射線、とくにα線の危険性がよく分かる論文です。α線を出す元素として、 などがあり、注意したいものです。 |